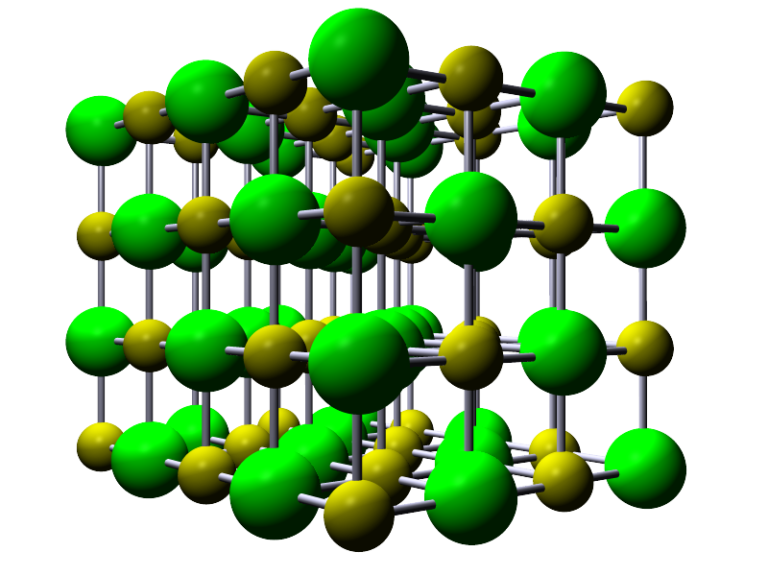
✅ Las sustancias iónicas están constituidas por iones positivos y negativos que forman una estructura cristalina rígida, con fuertes enlaces electrostáticos.
Las sustancias iónicas están constituidas por iones, es decir, átomos o grupos de átomos que han ganado o perdido electrones y, por lo tanto, poseen carga eléctrica. Estas sustancias se caracterizan por estar formadas por cationes (iones con carga positiva) y aniones (iones con carga negativa), que se atraen mutuamente por fuerzas electrostáticas. Esta atracción da lugar a la formación de una estructura ordenada y repetitiva conocida como red cristalina iónica.
Vamos a explorar con detalle cómo se conforman las sustancias iónicas y describiremos su estructura cristalina típica. Además, analizaremos las propiedades que derivan de esta organización y cómo influyen en su comportamiento físico y químico.
¿Qué son las sustancias iónicas?
Las sustancias iónicas son compuestos formados por iones con cargas opuestas que se mantienen unidos mediante enlaces iónicos. Estos enlaces resultan de la transferencia de electrones entre átomos, generalmente entre un metal y un no metal, donde el metal cede electrones y se convierte en un catión, mientras que el no metal recibe esos electrones y se convierte en un anión.
Formación de iones
- Cationes: Átomos que pierden electrones y adquieren carga positiva. Ejemplo: Na+, Ca2+.
- Aniones: Átomos que ganan electrones y adquieren carga negativa. Ejemplo: Cl–, SO42-.
Estructura de las sustancias iónicas
La disposición de iones en una sustancia iónica no es aleatoria, sino que forman redes cristalinas muy ordenadas. Cada ion se encuentra rodeado de iones de carga opuesta, las cuales se organizan en un patrón tridimensional que maximiza las atracciones y minimiza las repulsiones.
Red cristalina iónica
La estructura típica de un sólido iónico es una red cristalina, donde los iones se encuentran en posiciones fijas formando un retículo. Esta organización se mantiene gracias a las fuertes fuerzas electrostáticas que unen los iones en un sistema estable. El tipo y tamaño de los iones condicionan el tipo de red que se forma.
Ejemplos comunes de estructuras cristalinas iónicas
- Estructura NaCl: Cada ion Na+ está rodeado por seis iones Cl– y viceversa, formando una red cúbica centrada en las caras.
- Estructura CsCl: En esta estructura, cada ion Cs+ está rodeado de ocho iones Cl– en un arreglo cúbico simple.
- Estructura ZnS (blenda): Es un ejemplo de estructura iónica con coordinación tetraédrica, aunque con un ordenamiento ligeramente diferente al NaCl.
Propiedades derivadas de la estructura iónica
La estructura cristalina de las sustancias iónicas determina muchas de sus propiedades físicas:
- Elevados puntos de fusión y ebullición: Debido a la fuerte atracción entre iones.
- Solidez y dureza: Las redes cristalinas son rígidas.
- Fragilidad: Al aplicar una fuerza, se pueden desplazar los planos iónicos y generar repulsiones entre iones de igual carga, provocando la fractura.
- Conducción eléctrica en estado fundido o disuelto: En estado sólido no conducen electricidad porque los iones están fijos, pero en solución acuosa o fundidos los iones se mueven y permiten la conducción.
Importancia del tamaño iónico y la coordinación en la formación cristalina
Cuando hablamos de la formación cristalina en sustancias iónicas, no podemos dejar de lado dos aspectos fundamentales: el tamaño iónico y el número de coordinación. Estos dos factores actúan como los arquitectos invisibles que determinan qué tan estable y compacto será el cristal resultante.
¿Por qué es crucial el tamaño iónico?
Los iones, esas pequeñas partículas cargadas, tienen radios diferentes, y esa diferencia influye directamente en cómo se organizan dentro de un cristal. Si los iones son muy desproporcionados en tamaño:
- Los iones grandes pueden dejar demasiado espacio vacío, haciendo que la estructura sea menos estable.
- Los iones pequeños pueden quedar «perdidos» en espacios demasiado grandes, lo que también afecta la cohesión.
Por eso, un balance justo entre la porción catiónica y aniónica es clave para lograr un empaquetamiento óptimo.
El papel de la coordinación en estructura iónica
El número de coordinación es el número de iones de carga opuesta que rodean a un ion dado. Esta es una pieza fundamental porque determina la geometría y la estabilidad del cristal.
Ejemplo de números de coordinación típicos
- Coordinación 6: típica en la estructura NaCl, donde cada ion está rodeado por seis iones opuestos.
- Coordinación 4: común en cristales tipo Zincblenda (ZnS), más compacta y con ángulos definidos.
- Coordinación 8: presente en la estructura CaF2, con una alta coordinación para el catión.
Relación entre radio iónico y coordinación
| Razón del Radio Catión/Anión | Número de Coordinación Favorable | Ejemplo Típico |
|---|---|---|
| 0.225 – 0.414 | 4 | Zincblenda (ZnS) |
| 0.414 – 0.732 | 6 | Halita (NaCl) |
| 0.732 – 1.000 | 8 | Fluorita (CaF2) |
Esta tabla nos muestra que a medida que el catión se hace más grande respecto al anión, la coordinación tiende a aumentar, permitiendo estructuras más compactas y estables.
Un vistazo a cómo el tamaño marca la diferencia
- Demasiado pequeño: El catión no llena el espacio, provocando inestabilidad o estructuras menos densas.
- Demasiado grande: No permite una coordinación alta, limitando la cantidad de vecinos aniónicos y afectando la estabilidad.
Así, la formación de cristales iónicos no es un simple amontonamiento de iones, sino un delicado juego de proporciones y conexiones que determina su estructura, propiedades y resistencia.
Preguntas frecuentes
¿Qué son las sustancias iónicas?
¿Cómo es la estructura de una sustancia iónica?
¿Por qué las sustancias iónicas tienen altos puntos de fusión?
| Punto Clave | Detalle |
|---|---|
| Formación | Se forman por transferencia de electrones entre metales y no metales, generando iones. |
| Iones | Catión (carga positiva) y anión (carga negativa), se atraen electrostáticamente. |
| Estructura | Red cristalina tridimensional ordenada, ejemplo: cloruro de sodio (NaCl). |
| Propiedades físicas | Sólidos a temperatura ambiente, altos puntos de fusión y ebullición, duros y quebradizos. |
| Conductividad eléctrica | Conductores cuando están disueltos en agua o fundidos, no en estado sólido. |
| Solubilidad | Generalmente solubles en agua debido a la polaridad y capacidad de ionización. |
| Ejemplos comunes | NaCl, KBr, CaO, MgF2. |
| Importancia | Esenciales en procesos biológicos, industriales y en la formación de minerales. |
¿Te quedó alguna duda? Dejá tus comentarios abajo y no te olvides de revisar otros artículos en nuestra web que pueden interesarte.