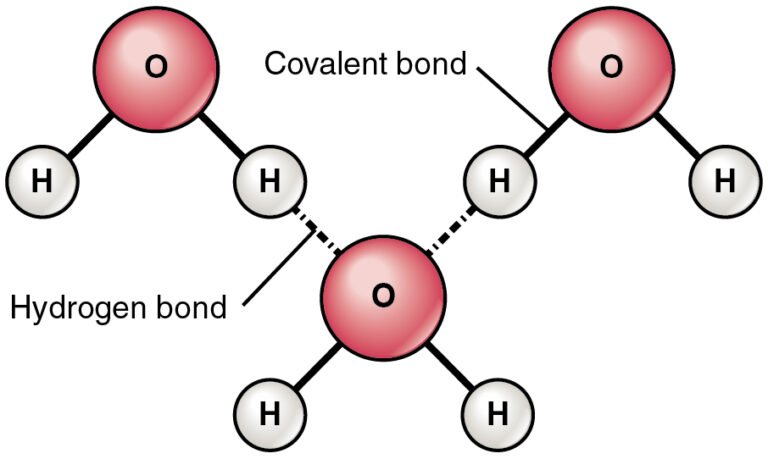
✅ El agua tiene bajo grado de ionización porque solo una pequeña fracción se disocia en H⁺ y OH⁻. Esto implica baja conductividad y neutralidad esencial.
El agua tiene un bajo grado de ionización debido a su naturaleza molecular y la fuerte atracción entre sus propias moléculas, lo que limita la separación en iones. Esto significa que, en condiciones normales, una cantidad muy pequeña de moléculas de agua se disocia en iones H+ y OH–, implicando que el agua es un electrólito débil y un excelente medio para reacciones químicas y procesos biológicos.
En este artículo analizaremos en detalle las razones detrás del bajo grado de ionización del agua, la importancia de este fenómeno y sus implicancias, desde la química básica hasta su impacto en la vida cotidiana y el equilibrio químico. Comprender esto nos ayudará a comprender fenómenos fundamentales como el pH, la conductividad eléctrica y el comportamiento de soluciones acuosas.
¿Qué es la ionización del agua?
La ionización del agua se refiere al proceso por el cual una pequeña fracción de moléculas de agua se separa en iones cargados. La reacción química que define este equilibrio es:
H2O (l) ⇌ H+ (ac) + OH– (ac)
Sin embargo, esta ionización no es completa ni muy frecuente, ya que la gran mayoría de las moléculas permanecen intactas.
Razones del bajo grado de ionización en el agua
1. Enlace covalente y polaridad de la molécula
Las moléculas de agua están formadas por átomos de hidrógeno y oxígeno unidos mediante enlaces covalentes polares. Esto genera una fuerza atractiva interna fuerte que mantiene unidas las moléculas y dificulta la separación en iones.
2. Fuerzas de atracción intermoleculares (puentes de hidrógeno)
Los puentes de hidrógeno entre las moléculas de agua generan una red de interacciones que desplazan el equilibrio hacia la forma molecular no ionizada, estabilizando la estructura líquida y limitando la cantidad de iones libres.
3. Constante de ionización muy baja (Kw)
La constante de ionización del agua (Kw) a 25 °C es de aproximadamente 1 × 10-14. Esto refleja la muy baja concentración de iones H+ y OH– en equilibrio, con una concentración molar de estos iones de aproximadamente 1 × 10-7 M en agua pura.
¿Qué implica el bajo grado de ionización del agua?
1. Neutralidad y el valor del pH
Debido a que el agua produce cantidades iguales de iones H+ y OH–, el pH del agua pura es 7, considerado neutro. Esto tiene gran importancia para la regulación química en sistemas biológicos y procesos industriales.
2. Conductividad eléctrica baja
Con tan pocas partículas cargadas (iones) libres en solución, el agua tiene una baja conductividad eléctrica, a diferencia de soluciones con electrolitos fuertes.
3. Mediador químico eficiente
El bajo grado de ionización permite que el agua funcione como medio para reacciones químicas sin interferir demasiado o cambiar significativamente el equilibrio de estas.
Cómo afecta el grado de ionización a otras propiedades del agua
- Capacidad buffer: Al tener un equilibrio muy estable entre iones, el agua ayuda a mantener el equilibrio ácido-base en sistemas acuosos.
- Solubilidad de sustancias: El grado de ionización limita la formación de iones de otras sustancias, afectando su solubilidad.
- Interacciones biológicas: El equilibrio iónico del agua es fundamental para funciones celulares y procesos metabólicos.
Importancia del equilibrio iónico en sistemas biológicos y ambientales
El equilibrio iónico es una cuestión fundamental tanto para los organismos vivos como para los ecosistemas. Este equilibrio determina cómo las moléculas, especialmente el agua, interactúan dentro de los sistemas biológicos y en el entorno natural.
¿Por qué es vital este equilibrio?
- Homeostasis celular: Las células mantienen su funcionamiento gracias al control estricto de los iones disueltos, como Na+, K+, Ca2+ y Cl–.
- Transporte de nutrientes: La osmolaridad del medio influye en la absorción de sustancias esenciales.
- Actividad enzimática: Muchas enzimas requieren concentraciones iónicas específicas para su correcta función catalítica.
- Regulación del pH: La presencia de iones H+ y OH– es crucial para mantener el pH, lo que impacta en reacciones químicas y estabilidad molecular.
Impacto en sistemas ambientales
En ambientes como lagos, ríos y océanos, el equilibrio iónico del agua determina la calidad del agua y la sobrevivencia de especies acuáticas.
- Contaminación: El desequilibrio iónico puede generar toxicidad por exceso de metales o compuestos ionizados.
- Biodegradación: Microorganismos dependen de condiciones iónicas estables para degradar materia orgánica.
- Ciclos bioquímicos:
- Ciclo del nitrógeno
- Ciclo del carbono
- Ciclo del fósforo
todos estos procesos requieren perfiles iónicos equilibrados para funcionar plenamente.
Tabla: Principales iones y sus roles en sistemas biológicos
| Ion | Función principal | Ejemplo en sistemas biológicos |
|---|---|---|
| Na+ | Regula presión osmótica y volumen celular | Impulsa señales nerviosas |
| K+ | Mantiene potencial de membrana | Contracción muscular |
| Ca2+ | Señalización intracelular | Coagulación sanguínea |
| Cl– | Balance eléctrico y pH | Digestión gástrica (ácido clorhídrico) |
Preguntas frecuentes
¿Qué significa que el agua tenga un bajo grado de ionización?
¿Cómo afecta el bajo grado de ionización del agua a su pH?
¿Por qué es importante el bajo grado de ionización para la vida?
| Punto Clave | Descripción |
|---|---|
| Ionización del agua | Es la disociación de moléculas de agua en iones H+ (protones) y OH- (hidroxilos). |
| Constante de ionización (Kw) | En agua pura, Kw ≈ 1×10^-14 a 25ºC, indicando baja ionización. |
| Grado de ionización | Extremadamente bajo, aproximadamente 1 cada 10 millones de moléculas se ionizan. |
| Implicancias en el pH | Concentra los iones H+ y OH- equilibradamente, resultando en pH neutro. |
| Importancia para la química | Permite que el agua sea un solvente estable para reacciones químicas biológicas y ambientales. |
| Influencia en organismos vivos | El pH estable permite el correcto funcionamiento de enzimas y procesos metabólicos. |
| Factores que afectan la ionización | Temperatura y presión pueden modificar el equilibrio de ionización. |
Te invitamos a dejar tus comentarios abajo y revisar otros artículos en nuestra web que seguramente te interesarán.