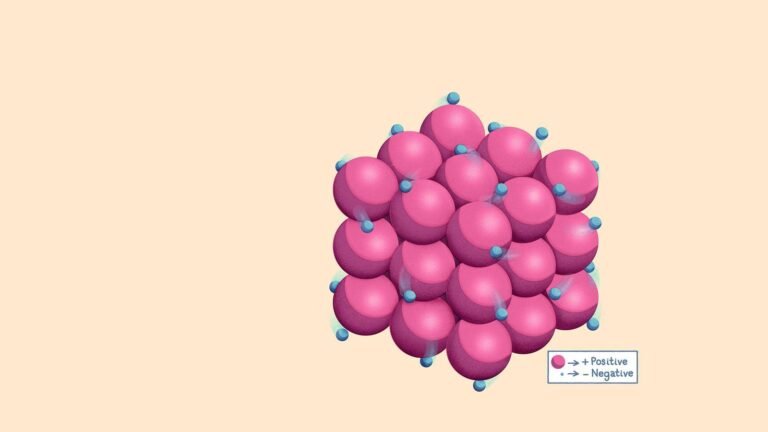
✅ Una unión metálica en estructura de Lewis es la atracción entre iones positivos y electrones libres. Identificala por el mar de electrones móviles.
Una unión metálica en la estructura de Lewis se refiere a la forma en que los átomos de metales comparten electrones para formar un enlace que mantiene unidas a las partículas dentro de un metal. A diferencia de los enlaces covalentes o iónicos, en la unión metálica los electrones de valencia se deslocalizan, formando un «mar de electrones» que rodea a los núcleos de los átomos metálicos y confiere a los metales sus propiedades características.
En este artículo exploraremos en detalle qué es una unión metálica, cómo se representa y se identifica en las estructuras de Lewis, y cuáles son sus propiedades más importantes. Además, entenderemos la diferencia con otros tipos de enlaces y cómo esta unión influye en la conductividad, maleabilidad y otras características de los metales.
¿Qué es una Unión Metálica?
La unión metálica es un tipo de enlace químico que se presenta en los metales puros y en algunas aleaciones. En este tipo de unión, los átomos metálicos pierden sus electrones de valencia, los cuales quedan libres y se mueven alrededor de núcleos positivos formando una nube o mar de electrones deslocalizados. Esta deslocalización facilita que el material mantenga su estructura sólida y le otorgue propiedades especiales.
Características de la Unión Metálica
- Electrones deslocalizados: Los electrones no están unidos a un átomo en particular, sino que se mueven libremente por toda la estructura metálica.
- Enlaces no direccionales: A diferencia del enlace covalente, la unión metálica no tiene una dirección fija, lo que permite la maleabilidad y ductilidad.
- Alta conductividad: La movilidad de los electrones facilita la conductividad eléctrica y térmica típica en metales.
Cómo Representar e Identificar la Unión Metálica en una Estructura de Lewis
En las estructuras de Lewis convencionales, se representan enlaces covalentes mediante pares de electrones compartidos entre átomos. Sin embargo, en el caso de la unión metálica, esta representación es más conceptual, ya que no podemos dibujar pares de electrones particulares sino una nube de electrones deslocalizados.
Pasos para Identificar la Unión Metálica:
- Reconocer átomos metálicos: Normalmente se trata de elementos del bloque d o s, como hierro (Fe), cobre (Cu), aluminio (Al), etc.
- Observar la estructura cristalina: La unión metálica se presenta en redes cristalinas compactas donde todos los átomos comparten estos electrones.
- Verificar la ausencia de pares de electrones fijados: A diferencia de enlaces covalentes, no se asignan pares específicos.
Por ejemplo, en el caso del cobre sólido, podemos pensar que todos sus átomos aportan electrones de valencia que forman un mar electrónico donde la carga negativa rodea los núcleos positivos organizados en una red cristalina.
Diferencias entre Unión Metálica e Iónica o Covalente
En los enlaces iónicos, los electrones se transfieren de un átomo a otro, y en los enlaces covalentes se comparten entre dos átomos específicos. La unión metálica, en cambio, se basa en electrones compartidos entre todos los átomos de manera global y no individual.
Comparación en tabla:
| Tipo de Enlace | Electrones | Direccionalidad | Ejemplo | Propiedades |
|---|---|---|---|---|
| Iónico | Transferencia completa | No direccional | NaCl | Alta solubilidad en agua, punto de fusión alto |
| Covalente | Compartidos entre átomos | Direccional | H2O, CH4 | Baja conductividad, formas moleculares definidas |
| Metálico | Electrones deslocalizados | No direccional | Cu, Fe, Al | Mala maleabilidad, alta conductividad térmica y eléctrica |
Importancia de la Unión Metálica en la Química y Materiales
La unión metálica es fundamental para explicar la maleabilidad, ductilidad, brillo y conductividad de los metales. Comprender esta unión permite también desarrollar nuevas aleaciones con propiedades mejoradas para la industria, la electrónica y la construcción.
La unión metálica es un concepto esencial dentro de la química y la física de los materiales que permite entender cómo se comportan los metales a nivel atómico y molecular.
Propiedades Físicas Derivadas del Mar de Electrones en Metales
Cuando hablamos del mar de electrones, nos referimos a esa nube móvil y deslocalizada de electrones libres que flotan alrededor de los átomos metálicos. Esta particularidad es la clave para entender un montón de características físicas que hacen a los metales tan especiales y útiles. Veamos cuáles son las más destacadas:
1. Conductividad Eléctrica y Térmica
- Electrones libres: Son los protagonistas aquí. Como se pueden mover fácilmente a través del metal, permiten que la electricidad circule sin problemas.
- Transmisión de calor: Esa misma movilidad electrónica también facilita que el calor se transfiera rápido, haciendo que los metales sean excelentes conductores térmicos.
- Ejemplo clásico: El cobre y la plata, con un mar de electrones super dinámico, llevan la delantera en esta categoría.
2. Maleabilidad y Ductilidad
Gracias a que los átomos no están rígidamente «pegados» gracias al mar de electrones, pueden deslizarse unos sobre otros sin romperse. Esto se traduce en:
- Maleabilidad: La capacidad de doblar o martillar los metales sin que se fracturen.
- Ductilidad: La posibilidad de estirar un metal en hilos finos (como el alambre) sin que se rompa.
Ejemplo Práctico
- El oro, que es extremadamente maleable, se usa en joyería porque se puede moldear fácilmente sin perder su integridad.
- El aluminio es otro ejemplo tipo por su ductilidad, usado en cables eléctricos y aviación.
3. Brillo Metálico
El mar de electrones también influye en cómo los metales reflejan la luz, generando ese
brillo característico que nos resulta tan atractivo visualmente.
¿Por qué sucede esto?
- Los electrones libres absorben y reemiten la luz en distintas longitudes de onda.
- Este proceso confiere a los metales su superficie brillante y lustrosa.
Resumen Rápido en Tabla
| Propiedad | Explicación | Ejemplo |
|---|---|---|
| Conductividad Eléctrica | Movilidad de electrones libres permite el paso eficiente de corriente. | Cobre, Plata |
| Conductividad Térmica | Electrones transportan calor rápidamente entre átomos. | Aluminio, Plata |
| Maleabilidad | Átomos se deslizan sin romper la estructura gracias al mar electrónico. | Oro, Cobre |
| Ductilidad | Se puede estirar en alambres finos sin deformarse. | Aluminio, Níquel |
| Brillo Metálico | Electrones reflejan la luz generando superficies brillantes. | Plata, Oro |
Preguntas frecuentes
¿Qué es una unión metálica?
¿Cómo se representa en la estructura de Lewis?
¿Cómo identificar una unión metálica en un compuesto?
| Punto Clave | Descripción |
|---|---|
| Definición | Enlace entre átomos de metales compartiendo electrones libres. |
| Electrones de valencia | Electrones deslocalizados que forman un «mar» alrededor de los núcleos. |
| Estructura de Lewis | No representa directamente la unión metálica, a diferencia de enlaces covalentes o iónicos. |
| Ejemplos | Metales puros como hierro, cobre, aluminio y aleaciones. |
| Propiedades | Conductividad eléctrica y térmica, maleabilidad y ductilidad. |
| Detectar unión metálica | Reconocer metales en su forma elemental o aleaciones, sin moléculas discretas. |
¿Te resultó útil esta información? Dejá tus comentarios y no te pierdas otros artículos en nuestra web que también pueden interesarte.