✅ El número atómico Z indica la cantidad de protones en el núcleo de un átomo, definiendo su identidad y propiedades químicas. ¡Clave esencial!
El número atómico Z indica la cantidad de protones que tiene un átomo en su núcleo. Este valor es fundamental para identificar el elemento químico, ya que cada elemento en la tabla periódica tiene un número atómico único. Además, en un átomo neutro, el número atómico también determina la cantidad de electrones en la nube electrónica, equilibrando la carga positiva del núcleo.
En este artículo vamos a profundizar en el significado del número atómico Z, su relación con las partículas subatómicas y cómo influye en las propiedades químicas de los elementos. Entender esta característica es clave para comprender la estructura atómica y la organización de la tabla periódica.
¿Qué es el número atómico Z?
El número atómico Z es un valor entero que representa la cantidad de protones en el núcleo de un átomo. Por ejemplo, el hidrógeno tiene Z = 1 porque tiene un solo protón, mientras que el oxígeno tiene Z = 8 ya que tiene ocho protones.
Esta cantidad es única para cada elemento y determina la identidad del mismo, ya que ningún otro elemento puede tener la misma cantidad de protones. Es una propiedad fundamental para distinguir un elemento de otro.
Relación entre el número atómico y las partículas en el átomo
Protones
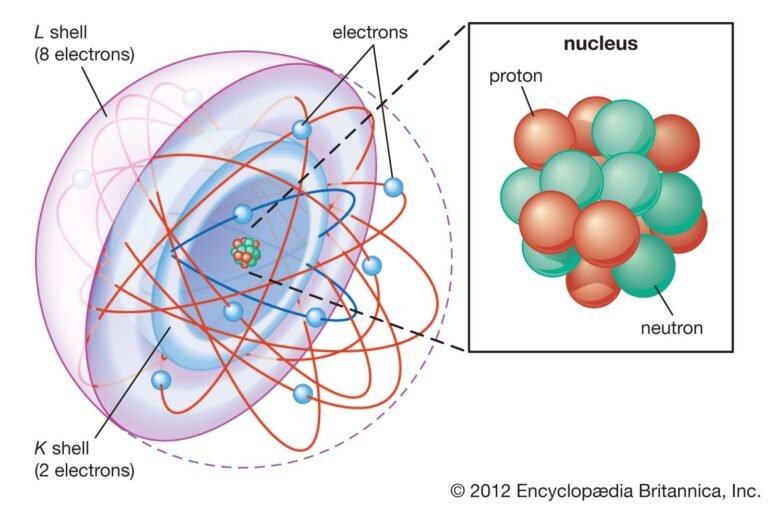
Los protones son partículas con carga positiva que se encuentran en el núcleo atómico. Su número es exactamente igual al número atómico Z, por lo que el número atómico indica cuántos protones hay en el núcleo.
Electrones
En un átomo neutro, la cantidad de electrones es igual a la de protones para mantener el equilibrio eléctrico. Por lo tanto, el número atómico también nos indica la cantidad de electrones en un átomo sin carga eléctrica.
Neutrones
Los neutrones son partículas neutrales que también habitan en el núcleo, pero su cantidad no está dada por el número atómico sino por el número másico (A), que es la suma de protones y neutrones.
Importancia del número atómico en la química y la física
El número atómico no solo establece la identidad del elemento, sino que influye en las propiedades químicas y físicas:
- Configuración electrónica: El número atómico determina cuántos electrones hay y, por lo tanto, su disposición en capas y niveles de energía.
- Reactividad química: La cantidad de electrones afecta cómo un átomo interactúa y forma enlaces con otros.
- Posición en la tabla periódica: Los elementos están ordenados según su número atómico, lo que refleja las tendencias periódicas en sus propiedades.
Resumen
El número atómico Z indica la cantidad de protones en el núcleo de un átomo y, en átomos neutros, también la cantidad de electrones. Es fundamental para definir la identidad del elemento y comprender su comportamiento químico y físico. Conocer y entender este concepto es básico para avanzar en el estudio de la química y la estructura atómica.
Cómo el número atómico afecta la formación de isótopos y su estabilidad nuclear
El número atómico (Z) no solo determina la identidad química de un elemento, sino que también tiene un papel crucial en la formación de isótopos y en la estabilidad nuclear de sus átomos. Vamos a desentrañar juntos esta relación fascinante.
¿Qué son los isótopos?
Antes que nada, recordemos que los isótopos son variantes de un mismo elemento que poseen igual número de protones (Z), pero distinto número de neutrones. Esto significa que comparten propiedades químicas, pero pueden presentar diferencias en propiedades físicas y nucleares.
Características principales:
- Igual número atómico (Z): determina el elemento químico.
- Diferente número másico (A): varía según la cantidad de neutrones.
- Estabilidad variable: algunos son estables, otros radiactivos.
¿Cómo influye el número atómico en los isótopos?
A medida que aumenta Z, el balance entre protones y neutrones debe ajustarse para mantener la estabilidad del núcleo. Esto se debe a que los protones, todos con carga positiva, se repelen entre sí, y es el papel del neutrón actuar como «pegamento nuclear» para contrarrestar esa repulsión.
Relación espacio-temporal entre protones y neutrones:
- Para elementos con Z bajo (ligeros), la cantidad de neutrones suele ser aproximadamente igual a la de protones (N ≈ Z).
- Para elementos con Z alto (pesados), la proporción de neutrones es mayor que la de protones (N > Z), para compensar la repulsión electrostática.
- Si el equilibrio se rompe demasiado, el átomo se vuelve inestable y puede sufrir decaimientos radiactivos.
Tabla comparativa: Proporción neutrones/protones según número atómico
| Rango de Número Atómico (Z) | Proporción Neutrones/Protones (N/Z) | Ejemplos de Isótopos Estables |
|---|---|---|
| 1 – 20 (Elementos ligeros) | ~1 | Carbono-12, Oxígeno-16, Calcio-40 |
| 21 – 50 (Elementos medios) | 1.2 – 1.3 | Hierro-56, Zinc-64 |
| 51 – 82 (Elementos pesados) | 1.3 – 1.5 | Plomo-208, Uranio-238 |
Impacto en la estabilidad nuclear
Cuando la proporción N/Z está fuera del rango óptimo, los núcleos intentan recuperarla a través de procesos de desintegración. Algunos de los modos principales son:
- Decaimiento beta (β):
- β⁻: un neutrón se transforma en protón, emitiendo un electrón.
- β⁺: un protón se convierte en neutrón, emitiendo un positrón.
- Emisión alfa (α): expulsión de una partícula alfa (2 protones y 2 neutrones) para reducir la masa y el número atómico.
- Captura electrónica: un protón capta un electrón para convertirse en neutrón.
Esto demuestra que el número atómico es la base para entender no solo “qué elemento tenemos”, sino también cómo se comportan sus isótopos y qué tan estables resultan en el tiempo.
Preguntas frecuentes
¿Qué es el número atómico Z?
¿El número atómico determina el elemento químico?
¿El número atómico indica la cantidad de electrones?
| Punto clave | Descripción |
|---|---|
| Número atómico (Z) | Indica la cantidad de protones en el núcleo del átomo. |
| Identificación del elemento | El número atómico define qué elemento químico es. |
| Estado de carga del átomo | En átomos neutros, Z = número de electrones; en iones, varía. |
| Diferencia con número másico (A) | El número másico suma protones y neutrones, mientras que Z solo protones. |
| Impacto en propiedades químicas | Determina la configuración electrónica y comportamiento químico. |
| Isótopos | Tienen igual Z pero distinto número de neutrones. |
Dejá tus comentarios y no te pierdas otros artículos interesantes en nuestra web.