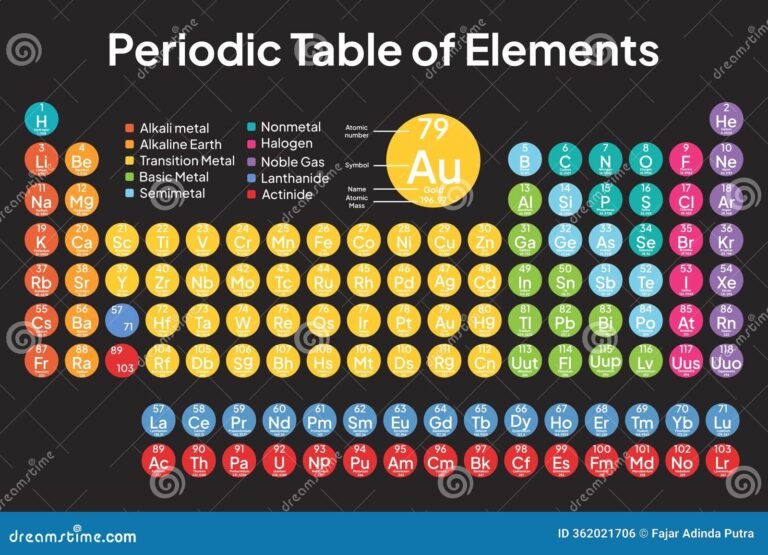
✅ Metales brillantes y conductores, no metales vitales y gases nobles inertes dominan la Tabla Periódica, clave para entender la materia y su energía.
En la tabla periódica, los elementos se clasifican principalmente en tres grandes grupos: metales, no metales y gases (que corresponden a un subconjunto de no metales conocidos como gases nobles y otros gases no metálicos). Esta clasificación se basa en las propiedades físicas y químicas de los elementos, como la conductividad, la apariencia, la maleabilidad y el estado físico a temperatura ambiente.
En este artículo vas a descubrir cómo identificar cada uno de estos grupos en la tabla periódica, qué características los diferencian y algunos ejemplos relevantes de cada categoría. También explicaremos por qué es importante entender estas distinciones para estudiar química y sus aplicaciones prácticas.
Clasificación de los Elementos en la Tabla Periódica
Metales
Los metales son la mayoría de los elementos en la tabla periódica. Se encuentran en el lado izquierdo y en el centro de la tabla, además del grupo del bloque f (los lantánidos y actínidos). Las características principales de los metales incluyen:
- Buen conductor de electricidad y calor.
- Superficie brillante y aspecto metálico.
- Maleables y dúctiles (se pueden moldear y estirar).
- Generalmente sólidos a temperatura ambiente (excepto el mercurio).
Ejemplos de metales comunes son:
- Hierro (Fe)
- Cobre (Cu)
- Oro (Au)
- Aluminio (Al)
- Zinc (Zn)
No Metales
Los no metales se encuentran principalmente en la parte superior derecha de la tabla periódica. A diferencia de los metales, los no metales suelen tener las siguientes características:
- Malos conductores de electricidad y calor (excepto algunos formadores de semiconductores).
- Superficie opaca y no metálica.
- Frágiles y no maleables cuando son sólidos.
- Presentan diferentes estados físicos a temperatura ambiente: sólidos, líquidos o gases.
Ejemplos de no metales incluyen:
- Carbono (C)
- Azufre (S)
- Fósforo (P)
- Oxígeno (O)
- Nitrógeno (N)
Gases
Dentro de los no metales hay un subgrupo muy importante: los gases nobles o gases inertes, ubicados en el grupo 18 de la tabla periódica. Son elementos gaseosos a temperatura ambiente, inertes y con poca reactividad química. Además, algunos otros no metales gaseosos forman parte del grupo de gases esenciales para la vida y diversas aplicaciones.
- Gases nobles: Helio (He), Neón (Ne), Argón (Ar), Kriptón (Kr), Xenón (Xe), Radón (Rn).
- Otros gases no metales: Oxígeno (O2), Nitrógeno (N2), Flúor (F2), Cloro (Cl2).
Tabla Resumen de Metales, No Metales y Gases en la Tabla Periódica
| Tipo | Ubicación en la tabla | Estado a temperatura ambiente | Ejemplos | Características principales |
|---|---|---|---|---|
| Metales | Izquierda y centro, bloques s, d y f | Sólidos (excepto Hg) | Hierro, Cobre, Oro, Aluminio | Conductores, brillantes, maleables |
| No Metales | Derecha superior | Sólidos, líquidos y gases | Carbono, Azufre, Fósforo | Aislantes, no brillantes, frágiles |
| Gases (subgrupo no metales) | Grupo 18 y algunos del grupo 17 y 16 | Gases | Helio, Neón, Oxígeno, Nitrógeno | Inertes o reactivos, no metálicos |
¿Por Qué Es Importante Conocer Esta Clasificación?
Entender cuáles son los metales, no metales y gases dentro de la tabla periódica es fundamental para comprender las propiedades físicas y químicas de los elementos, cómo se combinan para formar compuestos y sus aplicaciones industriales o biológicas. Esta clasificación también facilita el estudio de la química general, la física del estado sólido y la ingeniería de materiales, ya que cada grupo presenta comportamientos y usos industriales diferentes.
Diferencias en la Reactividad Química y Aplicaciones Tecnológicas de Cada Grupo
Cuando hablamos de reactividad química, entramos en un terreno donde los metales, no metales y gases nobles juegan roles tan distintos como una milanesa casera y una sushi de salmón fresco: ambos exquisitos, pero para gustos muy diferentes.
Reactvidad según el grupo: un vistazo rápido
- Metales: Poseen una reacción bastante enérgica, especialmente los alcalinos y los alcalinotérreos, con tendencia a perder electrones y formar cationes. ¡Cuidado al mezclar con agua!
- No metales: Generalmente buscan ganar o compartir electrones, mostrando una reactividad variable que puede ir desde el sutil oxígeno hasta el explosivo fluor.
- Gases nobles: Los reyes de la indiferencia química, mostrando una reactividad casi nula, aunque bajo condiciones extremas pueden formar compuestos sorprendentes.
Tabla comparativa de reactividad química
| Grupo | Características de Reactividad | Ejemplos | Riesgo en Reacción |
|---|---|---|---|
| Metales | Pierden electrones con facilidad, formando iones positivos (cationes) | Hierro (Fe), Sodio (Na), Aluminio (Al) | Alto, pueden generar chispas y reaccionar con agua |
| No Metales | Ganan o comparten electrones, formando aniones o enlaces covalentes | Oxígeno (O), Cloro (Cl), Fósforo (P) | Variable, desde baja a extremadamente alta (fluor) |
| Gases Nobles | Tendencia a no reaccionar; tienen capa electrónica completa | Helio (He), Neón (Ne), Argón (Ar) | Bajo, muy estables |
Aplicaciones Tecnológicas: ¿Dónde brilla cada uno?
Así como cada uno tiene su personalidad, también brilla en distintas tecnologías y usos cotidianos:
- Metales:
- Construcción y estructura: hierro, acero y aluminio dominan el rubro.
- Energía: cobre en cables y litio en baterías recargables.
- Innovación tecnológica: titanio en aeroespacial, oro en dispositivos electrónicos.
- No Metales:
- Salud y medicina: oxígeno para terapias respiratorias, yodo en desinfectantes.
- Química industrial: cloro en producción de plásticos, fósforo en fertilizantes.
- Alimentos y agricultura: nitrógeno para conservar alimentos y fertilizantes nitrogenados.
- Gases Nobles:
- Iluminación: neón en letreros luminosos, argón en lámparas fluorescentes.
- Protección atmosférica: gases inertes para soldadura y ambiente controlado.
- Medicina: helio en resonancias magnéticas y criogenia.
Resumen dinámico de aplicaciones y ventajas
| Grupo | Ventajas | Aplicaciones Clave |
|---|---|---|
| Metales | Alta conductividad, maleabilidad, resistencia | Infraestructura, electrónica, transporte |
| No Metales | Gran versatilidad química y biológica | Medicina, agricultura, industria química |
| Gases Nobles | Estabilidad, baja reactividad, propiedades físicas únicas | Iluminación, atmósferas protectoras, tecnología médica |
Preguntas frecuentes
¿Qué metales son más abundantes en la tabla periódica?
¿Cómo se identifican los gases en la tabla periódica?
¿Qué elementos no metálicos son esenciales para la vida?
| Tipo de Elemento | Ubicación en la Tabla | Ejemplos | Propiedades Clave |
|---|---|---|---|
| Metales | Parte izquierda y centro (Grupos 1-12, parte de los grupos 13-16) | Hierro (Fe), Cobre (Cu), Aluminio (Al), Oro (Au) | Conducen electricidad y calor, maleables, dúctiles, brillo metálico |
| No Metales | Parte superior derecha y algunas posiciones centrales | Carbono (C), Nitrógeno (N), Oxígeno (O), Azufre (S) | No conducen electricidad, variados estados a temperatura ambiente, más frágiles |
| Gases Nobles | Grupo 18, extremo derecho | Helio (He), Neón (Ne), Argón (Ar), Kriptón (Kr) | Inertes, bajas reactividades, gases monoatómicos a temperatura ambiente |
| Metaloides | Entre metales y no metales | Silicio (Si), Boro (B), Arsénico (As) | Propiedades intermedias entre metales y no metales |
Dejá tus comentarios abajo y no te pierdas otros artículos interesantes en nuestra web relacionados con la química y la tabla periódica.