Newsletter DPT Nro. 83
ISSN 2618-236X
Abril / 2023
NOTICIAS CIENTIFICAS
NOTICIAS CIENTIFICAS NACIONALES
Xenotrasplante de órganos porcinos para paliar la insuficiencia de donantes humanos de órganos
Evaluación comparativa de dos propuestas tecnológicas: (a) bioingeniería del genoma, y (b) bioingeniería del órgano
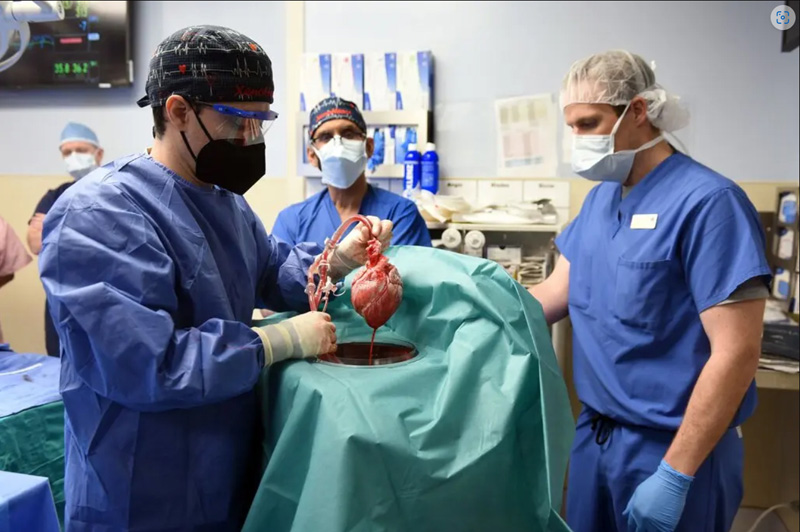
Cuando una persona padece problemas cardíacos, renales o hepáticos incompatibles con la vida, la solución indicada es hoy el trasplante de órganos provenientes de donantes humanos. En EE.UU. más de 115.000 personas están en listas de espera para recibir trasplante de órganos. Miles morirán antes de que llegue su turno, mientras que otros miles ni siquiera están incluidos en las listas, dada su remota posibilidad de acceder a un trasplante.
Como la disponibilidad de órganos humanos para trasplante es y será -en todo el mundo- sumamente escasa con relación a las magnitudes de necesidad y demanda, se considera a otras especies animales como una fuente alternativa de órganos. Muchas muertes podrían evitarse si se dispusiera de tecnologías adecuadas y seguras para el xenotrasplante, en humanos, de órganos provenientes de otras especies animales. El cerdo es una de las especies propicias, dado que el tamaño y fisiología de sus órganos son similares a los de humanos. De hecho, se utilizan comúnmente válvulas cardíacas de cerdo para sustituir a las humanas. En la actualidad se realizan experimentos de xenotrasplante de órganos porcinos con dos enfoques distintos: (a) bioingeniería del genoma, y (b) bioingeniería del órgano. A continuación presentamos una breve reseña de cada enfoque, con sus características, ventajas y debilidades.
(a) Bioingeniería del genoma porcino
Se trata aquí del trasplante de órganos provenientes de porcinos concebidos, gestados y criados específicamente como donantes para xenotrasplante. Con tal propósito, se modifica su genoma eliminando genes que puedan inducir el rechazo inmediato y añadiendo genes humanos que favorezcan la aceptación de los órganos por parte de los receptores. (1)
El primer paciente con quien se practicó este tipo de xenotrasplante fue el Sr. David Bennett. La Administración de Medicamentos y Alimentos (FDA) de EE.UU., que supervisa los experimentos de xenotrasplantes, autorizó el trasplante experimental -de emergencia por “uso compasivo”- por tratarse de un paciente con enfermedad cardiaca muy avanzada que no tenía otras opciones de tratamiento. El 7/01/2022, en el Centro Médico de la Universidad de Maryland (UM), se reemplazó su corazón defectuoso por el de un cerdo genéticamente modificado. Bennett falleció el 8/03/2022 (2 meses después del xenotrasplante); su corazón resultó afectado por el citomegalovirus porcino, una infección con efectos devastadores en los trasplantes (2) (3). El cerdo que actuó como donante del corazón, de 1 año y 109 kg, tenía 10 genes editados antes de su nacimiento. Por una parte, tenía inactivados 4 genes del genoma porcino: 3 de ellos implicados en el rechazo inmediato mediado por anticuerpos, para impedir el rechazo, y otro para prevenir el crecimiento excesivo del tejido cardiaco. Por otra parte, tenía integrados en su genoma 6 genes humanos que inducen la producción de proteínas relacionadas con la aceptación inmunitaria del órgano. Además se le suministraron fármacos para suprimir la reacción del sistema inmunitario. El corazón donado fue obtenido y provisto por la empresa Revivicor (con sede en Blacksburg, Virginia, EE.UU.) (4), especializada en crianza de porcinos genéticamente modificados para medicina regenerativa, con la colaboración del equipo de la Facultad de Medicina de la UM para evaluar la efectividad en primate humano del corazón de cerdo donado. La FDA está considerando si permitirá experimentos adicionales de xenotrasplante utilizando órganos de cerdos modificados genéticamente.
(b) Bioingeniería para la regeneración del órgano porcino
Una tecnología alternativa para el xenotrasplante es la bioingeniería para la regeneración de órganos porcinos, que no requiere cerdos concebidos, gestados ni criados específicamente como donantes, sino solo órganos porcinos provenientes de mataderos. El proceso de regeneración consiste esencialmente en someter a los órganos porcinos (por ejemplo: hígado, riñón, corazón) a “descelulización” y “recelulización”. Los pasos para ello son los siguientes: (a) disolver y eliminar las células del órgano, reduciéndolo a una estructura de andamiaje con sus vasos sanguíneos, y (b) Introducir, dentro de esa estructura, células vivas del órgano humano, las cuales fluyen hacia los ámbitos propicios del andamiaje para reiniciar las funciones del órgano (5) (6).
La empresa Miromatrix (Eden Prairie, Minnesota. EE.UU.) (7) prevé realizar, durante 2023, las primeras pruebas en humanos de órganos regenerados mediante bioingeniería. Si la FDA de EE.UU. presta su conformidad, el experimento inicial se realizaría acondicionando un hígado de cerdo regenerado para filtrar -externa y temporalmente- la sangre de un paciente hospitalizado con insuficiencia hepática aguda. Si ese experimento de “asistencia hepática” funcionara, podría intentarse un implante de órgano (probablemente riñón) regenerado mediante bioingeniería. El hígado ofrece la ventaja de ser el único órgano humano que puede autorrepararse y volver a crecer, mientras que la ventaja del riñón reside en que el paciente podría sobrevivir con diálisis si el implante fallara. Las células humanas necesarias para la recelulización provendrán de hígados y riñones donados que no pueden ser trasplantados (casi una cuarta parte de los riñones donados en EE.UU. son descartados porque no se los considera adecuados para trasplante, o porque no se encuentra un receptor compatible dentro del plazo establecido). Los biólogos de Miromatrix extraen las células utilizables de esos órganos donados y las multiplican en laboratorio. A partir de un órgano humano rescatado, la compañía podría cultivar suficientes células para repoblar varios andamiajes de hígado o riñón de cerdo.
El enfoque de Miromatrix surge de investigaciones realizadas a principios de la década de 2000, cuando Doris Taylor y Harald Ott, entonces en la Universidad de Minnesota, fueron pioneros en descelularizar completamente el corazón de una rata muerta y en sembrar el andamiaje resultante con células cardíacas inmaduras de ratas bebé que permitieron que el pequeño órgano latiera.
La bioingeniería para la regeneración de órganos es, probablemente, más viable y cercana que la bioingeniería del genoma porcino, ya que al eliminarse las células de cerdo se excluyen algunos de los riesgos de ese tipo de xenotrasplante, como virus animales al acecho o el hiperrechazo.
(*) En el Newsletter DPT Nº 67, Diciembre 2021, incluimos una reseña de varios artículos sobre “Quimerismo y xenoimplantes de órganos y tejidos provenientes de cerdos
Referencias:
(1) “Xenotrasplantes de órganos de porcinos en humanos: Hitos científico-tecnológicos con alto potencial traslacional” Newsletter DPT 70. Marzo 2022
(2) “Patient in Groundbreaking Heart Transplant Dies” By Roni Caryn Rabin. The New York Times, March 9, 2022
(3) “The gene-edited pig heart given to a dying patient was infected with a pig virus: The first transplant of a genetically-modified pig heart into a human may have ended prematurely because of a well-known—and avoidable—risk” By Antonio Regalado. MIT Technology Review. Biotechnology. May 4, 2022
(4) Sitio de la empresa Revivicor
(5) “Making pig livers humanlike in quest to ease organ shortage: Scientists are transforming pig livers to look and act like human ones, part of a quest to ease the nation’s organ shortage” By Lauran Neergaard. ABC News. December 27, 2022
(6) “Scientists are transforming pig livers into human-like ones to address organ shortage: Could this be the future of organ transplants?” By Loukia Papadopoulos. Interesting Engineering. Health. Dec 31, 2022
(7) Sitio web de la empresa Miromatrix Medical Inc.


