Newsletter DPT Nro. 67
ISSN 2618-236X
Diciembre / 2021
NOTICIAS CIENTIFICAS
RESEÑAS DE ARTICULOS INTERNACIONALES
Quimerismo y xenoimplantes de órganos y tejidos
Provenientes de cerdos
Solo en EE.UU más de 100.000 personas están esperando órganos imprescindibles para salvar sus vidas. Durante los últimos años, la cantidad de órganos disponibles se mantiene relativamente constante, mientras que la demanda aumenta de manera constante, debido particularmente al aumento de pacientes con enfermedades crónicas, asociado al envejecimiento de la población. Para reducir dicha brecha se propuso al cerdo doméstico como posible donante xenogénico de órganos para humanos. Con la aparición de técnicas avanzadas de edición y clonación de genes, ahora es posible eliminar los principales xenoantígenos y sobreexpresar varios transgenes humanos para mejorar la compatibilidad inmunológica y de coagulación entre cerdos y humanos.
Los cerdos exhiben, como donantes, notables ventajas sobre los primates no humanos: (a) dado que se producen para la alimentación, el uso de sus órganos genera menos preocupaciones éticas, (b) tienen camadas grandes, períodos de gestación cortos y crecen más rápido, (c) sus tejidos y órganos son compatibles, en mayor medida, con los humanos; por ejemplo: las válvulas cardíacas de cerdo se utilizan en humanos, la heparina (anticoagulante) se deriva de los intestinos de cerdo, los injertos de piel de cerdo se utilizan en quemaduras y se han utilizado córneas de cerdo para restaurar la vista, (d) son más fáciles de modificar genéticamente, y (e) pueden criarse con el grupo sanguíneo de donante universal. (*)
Esta reseña comprende tres (3) artículos referidos a xenoimplantes provenientes de cerdos. El primer artículo (1) se refiere a una innovación en quimerismo vascular. El segundo (2) trata sobre el trasplante de riñón de cerdo modificado genéticamente a una mujer en muerte cerebral. El tercero (3) focaliza en los trasplantes de piel y nervios de cerdos modificados genéticamente
1.- Primer artículo: Quimerismo vascular para la generación de órganos trasplantables (1.1.) (1.2.)
Como un método prometedor para generar órganos no inmunogénicos, a partir de donantes alogénicos y xenogénicos, se ha propuesto la descelularización por perfusión de órganos completos, seguida de recelularización con células derivadas de pacientes. Este enfoque se basa en la eliminación completa de las células y los antígenos del donante, pero la recelularización enfrenta desafíos importantes, como la necesidad de una cantidad suficiente de células y tipos de células necesarios para reconstruir un órgano completo. Con base en la literatura el equipo planteó la hipótesis de que reemplazar solo las células endoteliales del donante, mientras se mantiene el resto del órgano viable y funcional, podría ser técnicamente factible y podría proporcionar un atajo significativo en los esfuerzos para diseñar órganos trasplantables.
El proceso de rechazo comienza en el revestimiento interno de los vasos sanguíneos del órgano donante. Esa capa de células endoteliales avisa al sistema inmunológico acerca de la presencia de un órgano extraño, activándose así el proceso de rechazo. El equipo del Hospital Beilinson del Centro Médico Rabin (el centro de trasplantes más activo de Israel) consideró que no era necesario eliminar todos los materiales celulares y que sería más práctico extraer las células del revestimiento interno de los vasos sanguíneos y reemplazarlas por células derivadas de humanos que respondieran a los medicamentos contra el rechazo. Se trata de un atajo práctico y relativamente fácil de ejecutar en comparación con la construcción del órgano desde cero. Estos órganos híbridos podrían prepararse y almacenarse (con máquina de perfusión) de forma controlada hasta el momento en que sean requeridos para su implante.
Durante los últimos cuatro años el equipo perfeccionó su técnica innovadora para fabricar órganos híbridos. Pueden eliminar el revestimiento interno de los vasos sanguíneos de los pulmones, los riñones e incluso las extremidades de los animales y reconstruir el revestimiento utilizando células de placentas humanas. ¿Por qué se utilizan células de placenta humana?: (a) porque están disponibles en grandes cantidades, (b) porque la placenta es un órgano vascular que contiene lo requerido, y (c) porque las células de la placenta no son rechazadas (la madre no rechaza a su feto). Por tanto, es posible que los receptores de órganos híbridos no necesiten dosis elevadas de fármacos antirrechazo.
2.- Segundo artículo: Trasplantan un riñón de cerdo modificado genéticamente a una mujer en muerte cerebral (2.1.) (2.2.) (2.3.) (2.4.)
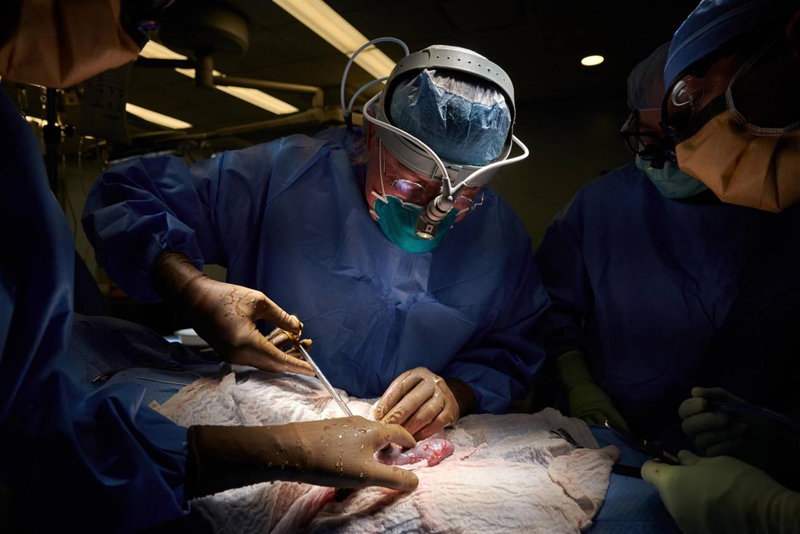
Un equipo quirúrgico liderado por el Dr. Robert Montgomery, del hospital Langone de la Universidad de Nueva York, logró trasplantar y hacer funcionar un riñón de cerdo modificado genéticamente en un cuerpo humano durante 54 horas. El avance podría significar dejar de depender de las donaciones humanas de órganos, ya que el xenotrasplante podría proveer una fuente prácticamente ilimitada de órganos para trasplante.
La operación, de dos horas de duración, se llevó a cabo el 25/09/2021 en el campus de Manhattan del Langone, y en ella se implantó el riñón de un cerdo genéticamente manipulado a una mujer en muerte cerebral, a quien (con el consentimiento de la familia) se mantuvo intubada durante 54 horas durante las cuales se estudió el nivel de desempeño del órgano porcino. Esto se consiguió mediante la neutralización del gen que codifica el glicano conocido como alpha-gal, que provoca un rápido rechazo de órganos porcinos. Los niveles de producción de orina y de creatinina fueron normales, lo que indicó un satisfactorio funcionamiento del riñón. Con el propósito de impedir una respuesta inmune del cuerpo humano, también fue trasplantada la glándula de timo del cerdo, encargada de “educar” al sistema inmune. El riñón fue unido a vasos sanguíneos en la parte superior de la pierna y cubierto con pantallas protectoras que permitieron observar al órgano y tomar muestras del mismo durante el estudio. Tampoco mostraron señales de rechazo las biopsias tomadas cada 12 horas y analizadas con microscopios.
Se trata de un importante paso adelante para hacer realidad la promesa del xenotrasplante. Los expertos señalan que las pruebas en primates no humanos y los experimentos con cuerpos humanos allanan el camino para los primeros trasplantes experimentales de riñón o corazón de cerdo en personas vivas en los próximos años. Aún no se dispone de datos difundidos en publicaciones científicas acerca del trasplante, y éste requerirá una rigurosa evaluación técnica.
3.- Tercer artículo: Trasplantes de piel y nervios de cerdos modificados genéticamente (3)
Si bien el trasplante de un riñón de cerdo modificado genéticamente a un receptor humano con muerte cerebral se difundió como una “nueva esperanza para un suministro ilimitado de órganos”, los cerdos modificados podrían tener usos inmediatos menos llamativos pero más efectivos, como donantes de injertos de piel y nervios, proveedores de válvulas cardíacas de larga duración y fuentes de carne libre de alergias.
El estudio de trasplante, realizado en la Universidad de Nueva York (NYU), mostró que el sistema inmunológico humano no rechaza inmediatamente un órgano de un cerdo diseñado para carecer de alfa-gal. El riñón porcino filtró los desechos de la sangre y produjo orina durante al menos 54 horas. Pero esos hallazgos no son novedosos; los experimentos con monos ya habían demostrado que los riñones de cerdo (como el que recibió la mujer con muerte cerebral) generalmente duran hasta una semana sin problemas, pero los órganos (que deben durar varios años) no son una opción viable para los xenotrasplantes. Los expertos señalan que también deberían purgarse genéticamente otras moléculas que tienen efectos inmuno-desencadenantes similares. Además, es posible que sea necesario agregar varios genes humanos al genoma del cerdo para moderar aún más la reacción inmunológica del cuerpo.
Pero los cerdos diseñados son prometedores para otras aplicaciones médicas con menos posibilidades de rechazo inmunológico que podrían marcar una gran diferencia; por ejemplo: válvulas cardíacas de reemplazo, piel para víctimas de quemaduras y como fuente de neuronas para tratar lesiones de nervios periféricos.
Referencias:
(1.1.) Fuente primaria: “Generation of vascular chimerism within donor organs” Shahar Cohen, Shirly Partouche, Michael Gurevich, Vladimir Tennak, Vadym Mezhybovsky, Dmitry Azarov, Sarit Soffer-Hirschberg, Benny Hovav, Hagit Niv-Drori, Chana Weiss, Adi Borovich, Guy Cohen, Avital Wertheimer, Golan Shukrun, Moshe Israeli, Vered Yahalom, Dorit Leshem-Lev, Leor Perl, Ran Kornowski, Arnon Wiznitzer, Ana Tobar, Meora Feinmesser, Eytan Mor, Eli Atar & Eviatar Nesher. Scientific Reports. Volume 11, Article number: 13437 (2021). Article. Open Access.- Published: 28 June 2021. DOI: 10.1038/s41598-021-92823-7
(1.2.) Fuente secundaria: “Scientists discover way to make pig organs compatible to humans” By Abigail Klein Leichman. Israel 21c. August 23, 2021
(2.1.) “Surgeons Successfully Transplanted a Pig Kidney into a Human Patient: and it worked” By Ameya Paleja. Interesting Engineering. Oct 20, 2021
(2.2.) “Pig-to-human transplants come a step closer with new test” By Carla K. Johnson. AP News. October 20, 2021
(2.3.) “Trasplantan con éxito un riñón de cerdo modificado a una mujer en muerte cerebral”. Boletín SINC – Ciencias Clínicas. EFE 22/10/2021
(2.4.) “Doctors successfully attach a pig kidney to a human body: The feat, not yet published, would mark a first for xenotransplantation” By Jennifer Couzin-Frankel. Science. 20 Oct. 2021
(3.) “Skin, nerve transplants from genetically modified pigs could help humans, but organs are a way off: A pig’s kidney was transplanted to a cadaver, but researchers say cross-species organ swaps remain years away” By Elie Dolgin. Science. Nov 1, DOI: 10.1126/science.acx9527
(*) “Importance of the pig as a human biomedical model” Joan K. Lunney, Angelica Van Goor, Kristen E. Walker, Taylor Hailstock, Jasmine Franklin, Chaohui Dai. Science Translational Medicine. Vol 13, Issue 621. 24 Nov 2021. DOI: 10.1126/scitranslmed.abd5758


